تعریف الکل ها
الکل ها دسته ای از ترکیبات آلی با گروه ها هیدروکسیل (-OH) هستند. متانول (الکل چوب ) سادترین الکل است که کاربرد زیادی به عنوان سوخت و حلال دارد. اتانول (الکل غلات) که با فرایند تخمیر تهیه می شود کاربرد فراوانی در صنایع بهداشتی ، آرایشی و پزشکی دارد و عنوان یک سوخت دوستدار محیط در برخی از خودروهای دوگانه سوز به کار می رود. ایزوپروپیل الکل به عنوان ضدعفونی کننده پوست پیش از تزریق به کار می رود .
الکل ها با روش های مختلف تهیه می شوند و گروه هیدروکسیل می تواند به بسیاری از گروه های عاملی دیگر تبدیل شود. به این دلیل الکل ها ترکیبات سنتزی بسیار مفیدی هستند.
الکل ها از نظر ساختاری به سه گروه طبقه بندی می شوند.الکل نوع اول الکل هایی هستند که در آنها گروه هیدروکسیل به کربن نوع اول (کربنی که به یک اتم کربن دیگر متصل است) پیوند دارد. در الکل نوع دوم گروه هیدروکسیل به اتم نوع دوم و در الکل نوع سوم به کربن نوع سوم متصل است.
نام گذاری الکل ها
برای نام گذاری الکل ها بر اساس قواعد آیوپاک به روش های زیر عمل می کنیم:
- بلندترین زنجیره هیدروکربنی شامل گروه (-OH) را به عنوان زنجیر اصلی در نظر میگیریم.
- شماره گذاری زنجیر اصلی از طرفی است که به گروه (-OH) نزدیکتر است.
- نام هیدروکربن مربوط همراه پسوند -ول همراه با شماره ای که موقعیت (-OH) را در زنجیر اصلی مشخص می کند آورده می شود.
مثال های زیر نام گذاری الکل ها را بر اساس قواعد آیوپاک نشان می دهد.
خواص فیزیکی الکل ها
الکل ها به دلیل توانایی ایجاد پیوند هیدروژنی نسبت به هیدروکربن ها ی مشابه دمای ذوب و جوش بالاتری دارند.توانایی تشکیل پیوند هیدروژنی موجب شده است تا الکل های با جرم مولکولی پایین به خوبی در آب حل شوند. اما با افزایش طول زنجیر هیدروکربنی انحلال پذیری الکل ها در آب کم می شود.
روش های تهیه الکل ها
متانول در صنعت از واکنش گاز کربن مونوکسید و هیدروژن ایجاد می شود. این واکنش در دما و فشار بالا و در حضور کاتالیزگر انجام می شود و به یک واکنشگاه صنعتی مجهز نیاز دارد. گاز های هیدروژن و کربن مونوکسید مورد نیاز از واکنش زغال گداخته و بخار آب در شرایط کنترل شده به دست می آیند. اتانول از تخمیر بی هوازی قند و نشاسته در حضور مخمر نان ایجاد می شود. گرما دادن غلات و سپس افزودن جوانه جو که مالت نامیده می شود ، قسمتی از نشاسته را به قندهای ساده تر تبدیل می کند.سپس افزودن مخمر نان و گرم نگه داشتن محلول موجب تبدیل قند به اتانول می شود.
C6H12O6 ——> 2C2H5OH + 2CO2
الکل حاصل از تخمیر 12 تا 15 درصد الکل دارد ، زیرا مخمر نان نمی تواند در غلظت های بیشتر از این زنده بماند. تقطیر موجب افزایش غلظت الکل می شود. تقطیر محلول آب – اتانول نمی تواند غلظت اتانول را بیشتر از 95% اتانول افزایش دهد ، زیرا محلولی که 95% اتانول و 5% آب دارد در دمای پایین تری (78.15 درجه سانتی گراد) نسبت به آب خالص 100 درجه و اتانول خالص 78.3 درجه می جوشد. مخلوطی از مایعات که در دمای پایین تری نسبت به هریک از اجزا می جوشد ، آزئوتروپ با دمای جوش کمینه نامیده می شود. هنگامی که الکل مطلق (اتانول 100%) مورد نیاز باشد ، الکل 95% (موسوم به الکل سفید یا طبی ) را از ستون شامل یک ماده جاذب آب مانند کلسیم اکسید خشک عبور می دهند. الکل تقلیبی (موسوم به الکل صنعتی ) با وارد کردن ناخالصی هایی مانند متانول ، متیل ایزوبوتیل کتون ، رنگ . غیره به الکل 95% ایجاد می شود تا قابل مصرف در نوشیدنی ها نباشد. بدیهی است این نوع الکل برای کاربردهای آزمایشگاهی هم نامناسب است.
همچنین اتانول در صنعت مستقیما از افزایش آب به اتیلن در دما و فشار بالا در فاز گازی و با استفاده از یک کاتالیزگر مانند تنگستن اکسید یا P4O10 تهیه می شود.
یکی از دلایلی که الکل ها حد واسط های سنتزی مفیدی هستند این است که میتوانند مستقیما از انواع بسیار زیادی از ترکیبات آلی دیگر سنتز شوند. در این مقاله تعدادی از مهم ترین روش های سنتز الکل ها را بررسی می کنیم.
افزایش آب به آلکن ها
با افزایش آب به آلکن ها در حضور یک اسید ، الکل تولید می شود. افزایش آب مطابق قاعده مارکونیکوف انجام می شود.
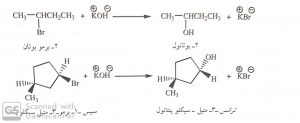
آبکافت آلکیل هالید ها
آلکیل هالیدها در واکنش جانشینی با یون هیدروکسید ، الکل تولید می کنند. واکنش از نوع هسته دوستی است که با حمله یون هیدروکسید به کربن شامل گروه ترک شونده انجام می گیرد.
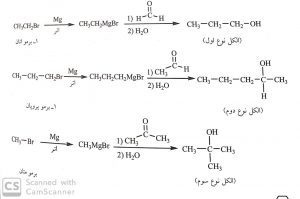
واکنش واکنشگرهای گرینیارد با گروه کربنیل
از واکنش واکنشگرهای گرینیارد با گروه کربنیل ، الکل تولید می شود . و این واکنش ها معمولا در حلال اتر کاملا خشک انجام می شوند، زیرا واکنشگرهای گرینیارد به رطوبت و آب حساس اند و در حضور رطوبت یا آب فعالیت خود را از دست می دهند. از واکنش واکنشگرهای گرینیارد با فرمالدهید ، الکل نوع اول ، آلدهید ها الکل نوع دوم و با کتون ها الکل نوع سوم ایجاد می شوند.
کاهش گروه کربنیل
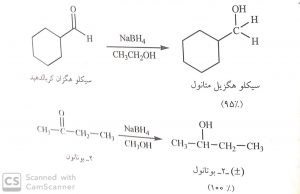
واکنشگرهای دهنده هیدرید ، گروه کربنیل را به یون آلکوکسید مربوط می کاهند که پروتون دار شدن ان در مرحله بعد موجب تولید الکل می شود. سدیم بورهیدرید (NaBH4) و لیتیم آلومنیوم هیدرید (LiAlH4) از مفیدترین واکنش گرهای دهنده هیدرید هستند که کاهش گروه کربنیل را با بهره خوبی موجب می شوند. این واکنشگرها ، هیدرید های کمپلکس نامیده می شوند ، زیرا ساختار ساده ای ندارند. در عوض اتم هیدروژن در آنها با پیوند اشتراکی به اتم بور یا آلومینیوم متصل است و بار جزئی منفی دارد . این آرایش موجب می شود تا هیدرید در انها خصلت هسته دوستی بیشتر و خصلت بازی کمتری نسبت به ساختار های ساده داشته باشد.
آلومنیوم نسبت به بور الکترونگاتیوی کمتری دارد بنابراین بار جزیی منفی بر روی هیدروژن در لیتیم آلومینیم هیدرید بیشتر است. در نتیجه لیتیم آلومینیم هیدرید کاهنده بسیار قوی تری است و کار کردن با آن نیز سخت تر است. لیتیم آلومینیم هیدرید با آب و الکل به طور انفجاری واکنش می دهد و گاز هیدروژن ازاد می کند . در صورتی که واکنش سدیم بور هیدرید با آب و الکل بسیار ملایم تر است . سدیم بور هیدرید یک کاهنده مناسب و بسیار گزینش پذیر است و آلدهید ها را به الکل های نوع اول و کتون ها را به الکل های نوع دوم تبدیل می کند. بهره های واکنش عموما عالی هستند.
سدیم بور هیدرید یک کاهنده گزینش پذیر است و با گروه های کربنیلی که فعالیت کمتری نسبت به آلدهیدها و کتون ها دارند به راحتی واکنش نمی دهد. بنابراین سدیم بور هیدرید می تواند آلدهید یا کتون را در حضور یک اسید یا استر بکاهد.
لیتیم بورهیدرید نسبت به سدیم بورهیدرید کاهنده قوی تری است. این واکنشگر به سهولت آلدهیدها و کتون ها و نیز ترکیباتی را که گروه کربنیل در آنها فعالیت کمتری دارند ، می کاهد.
لیتیم آلومینیم هیدرید ، کتون ها را به الکل های نوع دوم و آلدهید ها ، اسید ها و استرها را به الکل های نوع اول تبدیل می کند.
واکنش های الکل ها
گروه هیدروکسیل در الکل ها ره راحتی می تواند به هر گروه عاملی دیگر تبدیل شود.بنابراین الکل ها ترکیبات باارزشی هستند. دراینجا تعدادی از مهم ترین واکنش های الکل ها آورده شده است.
مکانیسم اکسایش الکل ها
اکسایش الکل ها با اکسنده های قوی مانند سدیم دی کرومات و سدیم پرمنگنات در محیط اسیدی یا بازی با اکسنده های ملایم مانند پیریدینیوم کلروکرومات (PCC) و پیریدینیوم دی کرومات (PDC) صورت می گیرد.هم PCC و هم PDC الکل های نوع اول را به آلدهید و الکل های نو دوم را به کتون اکسید میکنند. اکسنده های قوی تر مانند سدیم دی کرومات و سدیم پرمنگنات در محیط اسیدی یا بازی الکل های نوع اول را به کربوکسیلیک اسید و الکل های نوع دوم را به کتون اکسید می کنند. الکل های نوع سوم به طور معمول اکسید نمی شوند.
ساختار PCC و PDC در زیر نشان داده شده است :
PDC کمتر از PCC اسیدی است و بنابراین برای اکسایش ترکیبات حساس به اسید مناسب تر است.واکنشگر ملایم دیگر سوارن است که شامل DMSO (دی متیل سولفوکسید) به عنوان اکسید کننده است و همراه با اگزالیل کلرید 2(COCl) و تری اتیل آمین (Et3N) به کار می رود.این واکنشگر نیز الکل ها را به آلدهید و کتون اکسید می کند.
مثال های فوق نشان می دهد که نیتریک اسید ، اکسید فلزات واسطه و کاتیون های فلزات واسطه می توان به عنوان عامل اکسنده استفاده کرد. محلولی از کرومیک اسید رقیق در استون واکنشگر جونز نامیده می شود. محلول کروم تری اکسید در پیریدین واکنشگر کولینز نام دارد. این اکسنده ها هم نیاز از جمله اکسنده های قوی هستند.
تبدیل الکل ها به آلکیل هالیدها
واکنشگرهای مختلفی برای تبدیل الکل به الکیل هالید ها به کار می روند. هیدروکلریک اسید و هیدروبرومیک اسید در واکنش با الکل ها به ترتیب با الکل ها آلکیل کلرید و الکیل برمید ایجاد می کنند.
واکنش الکل ها با واکنشگرهای هالوژن دار کننده مانند PCl3 ، PCl5 ، PBr3 ، SOCl2 آلکیل هالیدها را ایجاد میکند. هالیدهای فسفر با بیشتر الکل های نوع اول و دوم بهره های خوبی دارند اما با الکل های نوع سوم به خوبی واکنش نمیدهند. واکنش با هیدروکلریک اسید و هیدروبرومیک اسید برای الکل های نوع سوم با بهره خوبی انجام میگیرد.
آب زدایی از الکل ها
آب زدایی از الکل ها به یک کاتالیزگر اسیدی نیاز دارد تا گروه هیدروکسیل الکل پروتون دار و به یک گروه ترک شونده خوب تبدیل شود. از دست دادن آب با از دست رفتن یک پروتون ادامه می باید و آلکن ایجاد می شود. بین واکنش دهنده ها و محصلات معمولا تعادل برقرار است.